Hirdetés
- Gurulunk, WAZE?!
- Luck Dragon: Asszociációs játék. :)
- Luck Dragon: Óraátállítás
- sziku69: Fűzzük össze a szavakat :)
- sziku69: Szólánc.
- gban: Ingyen kellene, de tegnapra
- D1Rect: Nagy "hülyétkapokazapróktól" topik
- Szoszo94: Xiaomi Mi Router 3G - Padavanra fel!
- Brain turbó: Intel Xeon CPU asztali alaplapban
- balojazz: Szódakészítés üzembiztosan és olcsón! Figyelem, csak hardcore szódázóknak!
Új hozzászólás Aktív témák
-

Szevam
senior tag
-

Szevam
senior tag
Sziasztok! Tud valaki ajánlani olyan laboreszköz boltot, ahol jó minőségű dolgokat adnak? (konkrétan csipesz és vegyszeres kanál kéne) Előre is köszönöm

-

emiki6
veterán
Na, látom nem túl aktív a topik, azért lementem, ha valaki írna valamit, lehet tudok rá reagálni. (Nem szándékosan írtam, de itt egész viccesen jött ki a mondat befejezése
 )
) -

fpeter07
veterán
Szerves kémia nevezetéktanhoz tudtok valami jól használható összefoglalást, ami leírja a szabályokat?
-

Mackósajt
senior tag
válasz
 Con Troll
#190
üzenetére
Con Troll
#190
üzenetére
Szükséges kiindulási adatok:
A KI molekulatömege: 166
A víz molekulatömege: 18Móltört 0,23 egyébként azt jelenti darabra a molekulák 23%-a KI.
A tömegszázalék tehát 0,23*166 / (0,23*166 + 0,77*18) * 100 = 73,37 m/m%
Megjegyzem, szerintem szobahőmérsékleten nem lehet ennyi KI-t feloldani vízben, de egy számítási példának végeredményben nem kell minden áron életszagúnak lennie...
-

Con Troll
senior tag
Sziasztok!
Ezt a faladatot el tudná magyarázni valaki, hogy hogyan kell megcsinálni? Biztos vagyok benne, hogy rém egyszerű, de nem tudok rájönni.Hány tömegszázalékos az a kálium jodid oldat, melynek móltörtje 0,23?
Köszönöm!
-

Mackósajt
senior tag
válasz
 fpeter07
#183
üzenetére
fpeter07
#183
üzenetére
Először is szem előtt kell tartani, hogy ez vizes oldatban van, mert ez nagyban meghatározza, hogy mi merre.
Ami keletkezik, az szárazanyagként felírva Na[Al(OH)4] lenne, de vizes oldatban ez ionjaira disszociált formában van jelen, mint ahogy a NaCl is Na+ és Cl- vízben, és a NaOH is Na+ és OH-. (És igen, az aluminátion pont ezért negatív töltésű, mert a benne lévő alumíniumion csak 3+.)
Az egész csak azért tűnhet furcsának, mert az egyenlet sűrítve foglal össze egy többlépéses reakciót (mint sok más egyenlet is). Ami itt történhet, az az, hogy a NaOH (pontosabban az OH-) először is leoldja az oxidréteget az alumíniumról (ha előkezelt a felhasznált alumínium, akkor ez a megelőző lépés kimarad), majd az alumínium reagál a vízzel hidrogénfejlődés közben (Al + 3 H2O = Al(OH)3 + 3H2), majd a keletkezett Al(OH)3 rögtön feloldódik a lúgoldatban (Al(OH)3 + OH- = [Al(OH4)]-.
A NaOH eleve disszociált formában van jelen, és maga a Na+ szigorúan véve sehol nem vesz részt a reakcióban, csak azért kell az összefoglaló egyenletbe, mert ott NaOH-ként van felírva a bal oldalra, és akkor kell a a jobb oldalra is.
-

fpeter07
veterán
2Al(s) + 2NaOH + 6H2O → 2Na+ + 2[Al(OH)4]- + 3H2(g)
Miért [Al(OH)4] keletkezik? (Al 3+)
-

fpeter07
veterán
Bodor Endre szervetlen kemia 1 könyvet hol lehet beszerezni digitalisan? Barmilyen forras erdekel.
-

thyeby
őstag
válasz
 PindurAnna
#180
üzenetére
PindurAnna
#180
üzenetére
Sziasztok!
Hátha ki tud valaki segíteni a következőkben:
Nagyon ráizgulam (nem csak egyedül) erre az eljárásra. Csak itthon nem kapható a hozzá szükséges szupergél.Az a lényege hogy x arányú izopropanolba keverünk a Dassos gélből,amit 4-6óra elteltéig fél óránkénti felrázással elegyítünk, és ezzel dolgozunk tovább. Mivel lehetne ezt a gigaszupergélt a hazai boltokból helyettesíteni?

-

PindurAnna
Közösségépítő
Sziasztok.
Gyermekem kémia versenyre készül: Miért is szeretem a kémiát? a dolgozata címe. Általános iskola 8.osztályos tanulója. Ehhez szeretnék segítséget kérni!
Tud valaki látványos és érdekes, esetleg otthon is elvégezhető kémia kísérletet? Természetesen úgy, hogy a lakás is megmaradjon
-

becuszabi
aktív tag
válasz
 Mackósajt
#178
üzenetére
Mackósajt
#178
üzenetére
Igen, az olcsó készülékházak polisztirolból, vagy azt is tartalmazó kopolimerből vannak. Öröm nézni, ahogy az aceton oldja

No, akkor mégis kapható? Jó pár éve még a híradásokba is bekerült pár idióta, amatőr, aki robbanószert csinált belőle és megsérült. Akkoriban leszedték a polcokról, de ezek szerint olcsóságának köszönhetően ismét visszakerült.
-

Mackósajt
senior tag
válasz
 becuszabi
#177
üzenetére
becuszabi
#177
üzenetére
Még kapható acetonos körömlakklemosó. Nemrég néztem, meg kicsit régebben (vagy 1,5 éve) vettem is. Műszaki cikkek tisztítására valóban nem a legjobb, mert egy csomó anyagot kikezd, olyan festékeket, bevonatokat ás műanyagokat is, amik az alkoholtól biztonságban vannak. (Viszont a laborban ez volt a legjobb az üvegedények tisztítására, már amikor nem kellett valami semmi igazán erős

-

becuszabi
aktív tag
A téli ablakmosó bőven elégnek kell lennie.
A sok mosószerrel szerintem az lehet a probléma, hogy -ahogy írtad is- bevonatot hagy a felületeken (az eredeti felhasználási területen ez ugye nem okoz problémát, hiszen leöblítjük).
A háztartási ablaktisztítóknak szinte ugyanez az összetétele, ugyanúgy van bennük alkohol, felületaktív anyag, illatanyagok stb.
Természetesen ez egy külön iparág, sok háttérkutatással, így ha korrektek akarunk lenni, akkor nem intézhetjük el azzal, hogy a főbb alkotók alapján egy kalap alá vonunk minden üvegtisztítószert (mint ahogy minden fa cellulóz rostokból áll, mégis hatalmas különbségek vannak köztük az eredetüktől függően).Acetont nem hiszem, hogy tennének bele, a gumi nem feltétlenül kedveli (nem azt mondom, hogy kioldaná a helyéről, de pl. képes azt megduzzasztani, amitől sérülékenyebbé válik).
Meg az acetont egyébként is igyekeznek mellőzni a hétköznapi életben (nem véletlen, hogy pl. az aceton tartalmú körömlakklemosó is kezd eltűnni, vagy talán már nem is kapható). -

thyeby
őstag
válasz
 becuszabi
#175
üzenetére
becuszabi
#175
üzenetére
Nagyon köszönöm a válaszaidat! Sokat segítettél a halovány látásomon.
Akkor tehát elég, ha felöntöm a flakont szélvédőmosóval (olcsóbb), és ha nehezen bírkózna a jéggel, akkor javítok rajta denaturált szesszel? Így, hogy mondod, a szélvédő mosó is prímán oldotta a jeget, csak azért nem éltem vele, mert macerás volt felhajtogatni az ablaktörlőket, hogy bőven priccolhassak a szélvédőre a tartályból. Ezt valójában azért nem alkalmaztam, mert csak sugárban fecskendezi az autó, s nem szétpermetezi a teljes felületen.A mosogatószerből miért baj, ha több van benne 1 ml-nél? Több szélvédőmosóval is az a bajom (pl a lidissel), hogy annyira "felületaktív", hogy este nem látok tőle az autópályán - még akkor se, ha szakad az eső. Képez valami ronda filmet az üvegen, amit csak kifejezetten üvegmosószerrel, és komoly izommunkával tudtam megszüntetni. Ezen lehet házilag javítani valami kemikália hozzáadásával? Más tekintetben elégedett voltam annak a szélvédőmosónak az árával is, és a hatásával is (mert a tecsógazdaságos mínusz 20 fokos pl. lazán belefagyott a rendszerbe már mínusz 10 foknál.)
És az üvegtisztítóknak mi a hatóanyaga? Pl a tükör ablaktiszítónak? Valami aceton? -

becuszabi
aktív tag
Az alkohol önmagában is fagyállóként hat. A jégoldóként használt folyadék gyakorlatilag ugyanaz, mint a téli szélvédőmosó, legfeljebb az alkoholtartalom tér el.
Azonos módon hatnak.
Kell bele:
víz
- ami ugye egyezik a jéggel, könnyen nedvesíti azt (gyorsan behatol a kristályok közzé)
- nagy a hőkapacitása (tömegéhez képest sok jeget tud felolvasztani)alkohol (kémiai szempontból a glikol is az)
- korlátlanul elegyedik a vízzel
- maradéktalanul elpárolog
- jelentősen csökkenti a víz fagyáspontjátezen kívül raknak hozzá egy kevés felületaktív anyagot (házi megoldás: max. 1 ml mosogatószer literenként), színezéket (hogy meg lehessen különböztetni az X terméket az Y-tól), meg illatanyagot, hogy tovább javítsák az egyedi jellemző = egyedi termék hatást
Régen a cégünknél került ki a gyártásból magas alkoholtartalmú folyadék, amit egyébként el kellett volna küldeni égetésre, mert már nem lehetett visszavinni és a regenerálása is sokba került volna...na ezt eladták olyan cégeknek, akik aztán konkrétan szélvédőmosót készítettek belőle. Gondolhatod milyen haszonkulccsal ment az üzlet.
-

thyeby
őstag
válasz
 becuszabi
#173
üzenetére
becuszabi
#173
üzenetére
Köszi!
Azért pontosítsunk:
A szélvédőmosó az, amit az ablaktörlő tartályába tankolunk, a jégoldóval viszont a befagyott ablaküvegeket jégmentesítjük. Szélvédőmosónak drága lenne 50%-os denaturált szesz oldat, hiszen 200 Ft/liter áron már nem csak tecsógazdaságoshoz juthat egy figyelmesebb autós, s abban még fagyálló is van.
Ami az illatát illeti, a legutóbb vásárolt jégoldóm szaga szinte egyezik a denszeszével - épp erről kaptam szagot. És eszembe jutott egy esetem, amikor a baumaxban vásároltam valami 800 pénzért egy fél liter penészeltávolító löttyöt. Amikor kipriccoltam, azonnal érezte az orrom, hogy ennek a hatóanyaga másítatlan hypo. Ki is próbáltam azonnal, mert az a fél liter gyakorlatilag semmire se volt elég. Tökéletesen egyként működtek. Míg előbbinek literje valami 50 forint, addig ugyanez penészkiller fantázianévre átkeresztelve több, mint ezerszeres haszonkulccsal elsózható. A marketinget úgy tanítják, hogy cukrot, lisztet mindenki el tud adni ott, ahol emberek élnek, egy jó marketinges viszont el tudja adni a sivatagban a homokot. És abban van az üzlet, mert cukrot, lisztet előbb termelni kell, homok viszont terem magától. No, ezt a tanítványok annyira mélyen be is vésik az agyukba, hogy mi szépen el is vagyunk árasztva ilyen marketing "termeléssel". -

becuszabi
aktív tag
Én vizsgáltam már ilyen löttyöt (szintén a helyettesíthetőség céljából).
Etilalkohol, etilénglikol ("fagyálló") és víz volt benne.A "metilén" valami fantázianév lehet, de kétlem, hogy metanol, mivel az nagyon erős méreg, ipari felhasználáson kívül nem nagyon lehet forgalmazni.
A denaturált szesz nagy része szintén etilalkohol és tesznek hozzá egy kevés, erős illatú oldószert, hogy ne legyen kellemes lehajtani belőle egy kupicával
Felhígítva (mondjuk 1:2 arányban vízzel, a szesz legyen a több) megfelel szélvédő mosónak, bár nem túl jó az illata. -

Mackósajt
senior tag
A metilén egy szabad gyök. Olyan reakcióképes, hogy gyanús, hogy nem lehet önállóan benne a flakonban. Nem véletlenül az csak az első tagja egy hosszabb vegyületnévnek? (Pl. a formaldehidet/metanal-t láttam már metilén-oxidnak írva.)
Annyi bizonyos, hogy a metilén nem ugyanaz, mint a metanol. Persze ki tudja mennyire volt eltévedve, aki a címkét írta. És simán el tudom képzelni, hogy metanol _is_ van benne.
A metanol a gumit elvileg nem oldja fel, bár lehet nem tesz jót, ha benne áll. A lakkról nem tudok nyilatkozni, fene se tudja miből van, nem értek a lakkokhoz, azok akár eltérően is reagálhatnak gyártmánytól függően.
-

thyeby
őstag
Sziasztok!
Az asztalos fórumon írtam egy egyszerű kérdést, onnan ide irányítottak a guruk.
Hogy gyorsabban végezzek, csak ctrl+c - ctrl+v lesz alább:
No, ennek a kérdésemnek csupán annyi köze lesz az asztalos szakmához, hogy akad néhány kolléga, aki télen is autóval jár, és nincs se szín, se garage, hanem reggelente kapari a jeget a szélvédőről.
Elég sok dologhoz konyítok, de a kémia világ életemben teljességgel kifogott rajtam. Tán akad egy autós, lovas, gyalogos asztalos, akinek nálamnál több affinitása van a kémia alapjaihoz.
Vettem én két spriccolós jégoldót. Nem spray-t, asztat nem szeretem, mert odafagy az ujjam hozzá, hanem pumpásat. Nem túl drágán, 450 pénzért darabját, mert ugye kapcsolatom van etéren.
Hamar fogy, reggelente két autót szaladok körbe vele. Amikor prickoltam, gyanúsan spiritusz szaga volt ennek a löttynek. Meg is néztem az összetevőit, nem-e véletlenül denaturált szesz a titok?
Valami 30-40 %-ban metilént tartalmaz. Megnéztem a denaturált szeszes flakonom tartalmát is. Az meg metilalkohol. Vakargattam a kopasz kobakomat: Nna, akkor ez most ugyanaz, vagy meg nemugyanaz? Hát itt tartok én alkímiából.
Mert ha ugyanaz, akkor egy liter denszesz árán három prickolós flakont is újra tudnék kotyvasztani, ráadásul denszeszt mindig tartok a műhelyben, mint remek gyantaoldót.Érzem, kicsit nevetséges a kérdésem - én már bután halok meg kémiailag. Egy rendőrviccet juttatott ez eszembe:
Előállít a rendőr egy teherautó sofőrt. Kérdezi a parancsnoka, hogy miért hozta be az ipsét?
- Igazoltatás során kérdeztem tőle, hogy mit szállít? Azt mondta, dzsemet. Gyanús volt nekem, hogy a szállítólevélre meg az volt írva, hogy jam. Felnéztem a platóra, hát ott meg egy csomó lekvár volt. Ez nem tiszta dolog!A denaturált szesz a jeget biztosan fel fogja oldani, de kérdés, hogy a lakkot és a szélvédőgumit is?
-

becuszabi
aktív tag
válasz
 nincsisbéla
#166
üzenetére
nincsisbéla
#166
üzenetére
A rajzot valószínűleg már megkaptad, amin láthatod az oktadekán szerkezetét.
A szerves molekulákat általában többféleképpen is fel lehet rajzolni, minél hosszabb a lánc, vagy több az elágazás, annál több variáció lehetséges. Ilyenkor természetesen az elnevezés is változik.
Ha van egy összegképleted és a lehetséges szerkezetet keresed, akkor vagy a google-t, vagy speciális adatbázisokat célszerű megkeresni.
Én ezt szoktam használni: http://www.chemspider.com/
Amúgy a C18H38 képletre történetesen 75 találatot dob ki -

nike_
addikt
válasz
 nincsisbéla
#168
üzenetére
nincsisbéla
#168
üzenetére
ja, értem, oké

egyébként küldöm neked a képet a C18H38-ról PÜ-ben.
-

nike_
addikt
válasz
 nincsisbéla
#166
üzenetére
nincsisbéla
#166
üzenetére
2-2-2 dimetil pentaoktán nem lehet, akkor már trimetil, az meg megint nem lehet, mert egy szénatomnak 4 kötése lehet, ebből 2-t bevisz a láncba, hogy folytatódhasson tovább, (kivéve a 2 szélső) ezért max. 2 elágazása lehet.
meg amúgy is, milyen pentaoktán?
 hány szénatomos az?
hány szénatomos az? -

nincsisbéla
aktív tag
válasz
 becuszabi
#165
üzenetére
becuszabi
#165
üzenetére
Köszi a választ, valóban nem izomer, én írtam rosszul.
Tényleg igazad van, ebből csak 1 jó! (azért is kérdeztem meg, mert nem voltam biztos abban hogy jó!)
Most azzal vagyok problémában hogy "rajzban" hogy néz ki. (c18h38-at többféle képen is le lehet rajzolni?)
Illetve hogy rajzoljak még ilyet (pl: a c19h39 hogy néz ki?) Esetleg ezt is tudod? [fénykép jöhet PÜ-ben]Azt tudom hogy így kell elnevezni őket, de ha másképp van a rajza akkor más a neve (2-2-2 dimetil-pentaoktán. [csak egy példa fejből, nem biztos hogy van ilyen])
Köszi, rég volt már ez na! (pár év alatt is mennyit felejt az ember, nemde?)
-

becuszabi
aktív tag
válasz
 nincsisbéla
#164
üzenetére
nincsisbéla
#164
üzenetére
Van két rossz hírem:
- ezek nem metán izomerek
- ha normál szénhidrogéneket akart a haverod kérni, akkor sem stimmel, mivel azoknak az általános képlete: C(n)H(2n+2), úgyhogy ennek csak a C18H38 felel megaz elnevezés a szénatomszám görögből eredő előtét alapján történik:
C10, deka, C10H22: dekán
C15, pentadeka, C15H32: pentadekán
stbC11H24: undekán, C18H38: oktadekán, C17H36: heptadekán
-

nincsisbéla
aktív tag
Egyik 12.-es haverom az imént hívott, hogy segítsek neki, mert én mindig is jó voltam kémiából.
Írjak neki metán izomereket.
Meg tudtam csinálni a c11h28-at, a c18h38-at, és a c17h38-at. De nem tudom hogy mi a nevük, mert már nem emlékszem hogy hogy kell őket elnevezni. Valaki? -

djSiku
csendes tag
Sziasztok!
Tudom, hogy nem szokás, most mégis, a segítségeteket szeretném kérni egy verseny kapcsán.
Iskolámban, a pécsi Pollack Mihály Műszaki Szakközépiskolában (kisPollack) 3 vegyész tagozatos társammal együtt egy kisfilmet készítettünk egy, az MTA Kémiai Kutatóközpont által kiírt videópályázatra.10 perces videónk látványos kémiai kísérleteket mutat be (ezüsttükör próba, cukor + tömény kénsav, cukor + kálium-klorát mint radikális oxidálószer, valamint füstbomba készítése), természetesen tanári lektorálással, a legteljesebb szakmaisággal. Mindezt egy fiktív környezetbe ágyaztuk, miszerint a reakciókat elszenvedő gumimacik a főszereplők, akik életre kelve fenyegetik az emberi társadalmat.. Igen poénos pillanatok vannak benne, a hozzá nem értőknek is érdemes megnézni..

A szakmai zsűri által kiosztott díjakon felül van egy közönségdíj, melyet a videók a nézőktől kapott lájkok száma alapján kaphatnak meg, ebben szeretnénk mindenki segítségét kérni.
A videó ezen a linken érhető el:
http://showyourscience.hu/2011/04/27/a-gumimacik-tamadasa-es-vegzete-i-ii-2/Kérem, hogy akinek van FaceBookja, az tegye meg ezt a 2 másodperces mozdulatot, hogy lájkolja (Tetszik-eli), mivel ez óriási segítség lenne kis csapatunk számára.
A videót egyébként a bama.hu is támogatja, elméletileg a napokban ott is meg fog rólunk jelenni egy cikk; valamint ha minden igaz és a Sors is úgy akarja, a Dunántúli Naplóban is lehet majd olvasni a kezdeményezésünkről.
Médiatámogatónk továbbá az erdélyi Zöld Nap Egyesület és a Garami Funky Staff Zenekar is (melynek a ClassFm műsorvezetője, Garami Gábor is tagja).A mi videónk egyébként kb 2 hetes csúszással került feltöltésre a többihez képest, azonban így is, 4 nap alatt több mint 370 lájkot sikerült összegyűjtenünk, ezzel az 5. helyen állunk a 35-ből. Az első helyen álló jelenleg körülbelül 930 lájkkal bír, így nagyon nagy szükségünk lenne a segítségre!
Köszönjük mindenkinek a közreműködést, és mégegyszer elnézést a nem egészen ide vágó témáért!
-

Mackósajt
senior tag
válasz
 cellpeti
#160
üzenetére
cellpeti
#160
üzenetére
Mármint úgy érted ha fel van írva az elektronhéj szerkeze? Jó volna, ha hoznál egy példát, mert még sose láttam "kvantumszámokkal megadva" egy elemet, az elektronszerkezeti jelölések közvetettebbek, különösen a végén (a spinkvantumszám nincs explicite jelölve bennük). + egy elemnek nincsenek ilyen kvantumszámai. Az azt felépítő egyes elemi részecskéknek, ppl. az egyedi elektronoknak van (ezért is tippelek arra, hogy talán az elektronhéj szerkezet eltérő jelölésű felírására gondolsz).
Azért találgatódzom neked egy sort:
- Ahány héj (főkvantumszám) van, annyiadik sor.
- Az utolsó héj alá tartozó alhéjjak (mellékkvantumszám) adja meg melyik mező. Ha csak s van, akkor s mező (a periódusos rendszer bal széle), ha p is van, akkor p mező (a táblázat jobb oldala), ha d is van, akkor d mező (a táblázat közepén lévő "híd"), stb. (Vigyázat, a d mezőtől kezdve trükkös dolgok vannak, de ezt nem kell tudni egy tiszta levezetésben...)
- A mezőn belüli oszlopszámot az adja meg, hogy az utolsó alhéjjon hány elektron van (mágneses és spinkvantumszám).Pl. a Nátrium: [Ne] 3s1 elektronszerkezet
Főkvantumszám: 3, a harmadik sorban van. (Egyben azt is jelenti, hogy a mellékkvantumszámok megengedett értékei 0,1,2 lehetnek)
Mellékkvantumszám: s vagyis 0. Az utolsó alhéj az 0-ás mellékvantumszámú (s), tehát a Nátrium az s mezőben van.
Mágneses kvantumszám: gondolom 0 lehet, mert nem lehet nagyobb az abszolút értéke, mint az adott elektronhoz tartozó mellékkvantumszám értéke.
Spinkvantumszám: ez ugye lehet -1/2 vagy 1/2. Ha mindkettő szerepel akkor 2 elektron van az utolsó energiaszinten, ha csak az egyik, akkor csak egy elektron van az utolsó energiaszinten. A Nátrium esetén csak egy elektron van, úgyhogy az s mező első sora lesz.
-

cellpeti
nagyúr
Sziasztok!
Honnan tudom melyik oszlopba és/vagy melyik sorba van az adott elem, ha:
- főkvantumszámmal
- mellékkvantumszámmal
- mágneses kvantumszámmal
- Spinkvantumszámmaladják meg?

-

cellpeti
nagyúr
válasz
 becuszabi
#155
üzenetére
becuszabi
#155
üzenetére
hát ennél.
Lenne még egy feladat. Én kiszámoltam, csak azt kéne le ellenőrizni, hogy jó-e, mert van feladatlap és azon más jött ki. (persze nem biztos, hogy az jó)
Állapítsuk meg, hogy a kiegészítendő SnO2+C = Sn + CO reakcióegyenlet szerint hány kg elemi szén szükséges 50kg ón(IV)-oxid redukálásához?
Atomtömegek:
Sn = 118,7; C=12; O=16Én így oldottam meg:
Ón-oxid képlete: SnO2, amelynek tömege: 150,7g -> 0,1507kg
Szén: C, amelynek tömege 12g -> 0,012kgMajd felírtam az összefüggést:
0,1507kg - 0,012
50kg - X
ebből lett, az hogy:0,1507*X = 0,012*50
0,1507*X = 0,6
X = 0,6/0,1507
X = 3,98kg -

becuszabi
aktív tag
válasz
 cellpeti
#152
üzenetére
cellpeti
#152
üzenetére
Közben még eszembe jutott, hogy az egészbe belerondíthat az ammónia azon tulajdonsága, hogy megfelelő hőmérsékleten és katalizátorként viselkedő szilárd anyagok jelenlétében képes elemeire bomlani.
Ebben az esetben pedig az is előfordulhat, hogy az elemi hidrogén részben redukálja a volfrám-oxidot, egy alacsonyabb oxidációs állapotú, de viszonylag stabil oxiddá, ami aztán ugyanúgy sav-bázis reakcióban reagál az ammóniával.
Jó lenne tudni, hogy ez az egyenlet milyen szövegkörnyezetben szerepelt.Az átmeneti fémek nagyon bonyolult reakciókra képesek (nem véletlenül használják elemi állapotban és vegyületeik formájában is számos folyamat katalizátoraként)
-

becuszabi
aktív tag
válasz
 cellpeti
#150
üzenetére
cellpeti
#150
üzenetére
Kicsit gondban vagyok

Nem a rendezéssel van a problémám, hanem a volfrám-nitrid képletével. Eddig úgy tudtam (meg meg is néztem), hogy a nitridekben a N oxidációs száma -3. Szóval vagy a képlet a rossz, vagy ez valójában egy keverék (mint ahogy a Fe3O4 is ténylegesen egy FeO-Fe2O3 összetételű oxid, úgy ez is lehetne egy WN-WN2 nitrid).
Ha ez utóbbit feltételezzük, akkor sikerült kifognod az egyenletrendezők rémálmát, a vegyes reakciókat
Szerintem ebben az esetben két reakció játszódik le. Van egyszer egy sav-bázis reakció (általában a nitridek keletkezése így történik) és van egy redox reakció, ahol a volfrám redukálódik, az ammónia nitrogénje pedig oxidálódik (ráadásul csak részben).
Nem vagyok 100%-ig benne biztos, de én a következőképpen vezetném le:
Ha a vegyes nitridre vonatkozó feltételezés igaz, akkor a WN-ben a W oxidáció száma +3, a WN2-ben pedig +6 (mint a kiindulási oxidban). A levezetést képként csatolnám, hogy a redox egyenletnél szemléletesebb legyen az elektronok mozgása): -
-

cellpeti
nagyúr
üdv
valaki el tudná nekem magyarázni a sztöchiometriai egyenletek rendezési elvét?

-

fpeter07
veterán
Nos... Ha nem kapok 5-ösnél rosszabb jegyet ebben a félévben, akkor esélyesen pályázok az 5-ösre. Próbálok nem hibázni.

-

fpeter07
veterán
A PH számítást hogy kell elvégezni?
Van egy ilyenem hogy: -log[H3O+]
Írtunk pár példát is:a) 0,01 mol/dm3 HCl
10^-2 mol/dm3
PH=2
b) 0,001 mol/dm3 HNO3
10^-3 mold/dm3
PH=3
c) 0,1 mol/dm3 NaOH
OH-= 10^-1
H3O+= 10^-13
PH= 13Az elsőből sikerült egy mintát leszűrnöm (10^-x), de a harmadik számomra egy kérdőjel.
-

Mackósajt
senior tag
válasz
 fpeter07
#141
üzenetére
fpeter07
#141
üzenetére
Azért "feleződik", mert nem mindegy, hogy oxigén molekula vagy oxigén atom. 1 oxigén molekula 2 atomot tartalmaz.
Számold össze az oxigént a reakcióegyenlet jobb oldalán. 8 O2 + 9 O = 12,5 O2 (25 O).
Az aláírt számításod helyesen 8x2 O + 18/2 O = 25 O vagy 8 O2 + 18/4 O2 = 12,5 O2.
-

fpeter07
veterán
Körülbelül egy éve nem rendeztem egyenletet, azóta már visszanéztem hogy mit, miért, hogyan kell.
Ez viszont nem világos:Oktán égése:
C8H18+12,5O2= 8CO2 + 9H2O
8*2+9O2= 25O2
Kérdésem az lenne hogy miért feleződik a bal oldalon?
-

becuszabi
aktív tag
válasz
 Anyimanyi
#135
üzenetére
Anyimanyi
#135
üzenetére
...akkor bővebben
Alapvetően onnan, hogy a vegyületek alkotói milyen oxidációs állapotban lehetnek. Vannak természetesen olyan elemek, amelyek több értéket is felvehetnek, attól függően, hogy milyen az elektronhéj szerkezetük, illetve milyen másik elemmel hozzuk össze. Az, hogy az adott párosításnál melyik vonzza a másik elektronja(i)t, az elem elektronegativitása határozza meg.
A feladatod megoldásánál előny, hogy a felsoroltak mindegyikénél van egy-egy olyan alkotó, ami csak adott számú elektront képes elveszíteni (vagy felvenni).oxidációs állapot - elektronegativitás
H: +1 (-1) .....................2,20
N: ±3, 5,4,2 ..................3,04
P: ±3, 5, 4 ....................2,19
O: -2 (-1) ......................3,44
Si: 4 ............................1,90
Ca: 2 ...........................1,00H2NO3: a legelektronegatívabb az O, így az oxidációs állapota -2, a 3-é -6, a N és a H is le fogja adni az elektronjait, azaz +1 és +5 lesz az állapotuk, a molekula csak úgy lesz semleges, ha a képlet HNO3 (salétromsav)...a H2NO3 ilyen formában tehát nem létezik
PH3: a P lehet 3 vegyértékű, a H csak 1, így létezhet a molekula (létezik is: foszfin)...az, hogy most ki kitől szed el elektront, annyira nem érdekes (az elektronok eloszlásában a P nemkötő elektronpárja is szerepet kap).
Ca2O: a Ca csak leadni tudja az elektronjait és csak kettőt, így egyértelmű, hogy csak a CaO összetételű vegyület létezik (kálcium-oxid), ez nem
SiH4: a Si csak 4 vegyértékű lehet, a H csak 1, létezhet a vegyület (és létezik is: szilán)
Azokban az esetekben, amikor az elektronegativitás értékei nagyon hasonlóak, a kötésben résztvevő elektronok amolyan közös tulajdonúak, a kötés kovalens jellegű lesz.
-

Anyimanyi
újonc
Sziasztok!
Honnan tudom,hogy egy adott vegyület létezik-e?
Pl. eladat
eladat arikázd be a nem létezőket!
arikázd be a nem létezőket!
1.H2NO3
2.PH3
3.Ca2O
4.SiH4
Az oxidációs számból vagy lerajzolva a szerkezeti képletükből?Vagy honnan?
Jah és a szigma és pi kötések száma és a nem kötő elektronok száma a központi atomon hány van?honnan tudom?
Előre is Köszi a Segítséget!
-
-

becuszabi
aktív tag
válasz
 Mackósajt
#131
üzenetére
Mackósajt
#131
üzenetére
A kálium-permanganát igen erős oxidálószer. Ha keletkezik is etén-diol, szerintem az sem a kettős kötés, sem a hidroxi csoportok miatt nem marad meg oxidatív közegben. Sőt az oxálsav sem túl stabil anyag, annak ellenére, hogy "sima" dikarbonsav, bizonyos körülmények között redukálószerként viselkedik. Szóval ha feltételezzük, hogy a feladatban szereplő képletek helyesek, akkor a reakció inkább valamiféle átmeneti állapotot ír le.
...mondjuk ha jobban belegondolok, akkor a gyakorlati preparatív munka során mi is többször jártunk már el úgy, hogy a reagáló anyagok megfelelő adagolásával az egyébként átmeneti állapotnak megfelelő végtermékeket kapjuk...azaz a telítetlen diol képződése elképzelhető.
-

Mackósajt
senior tag
válasz
 becuszabi
#130
üzenetére
becuszabi
#130
üzenetére
Nem túl részletezőek a források, mert egyrészt azt írják, hogy az alkinok oxidációs reakcióiban általában felhasad a hármas kötés, és két karbonsav keletkezik, de van olyan, ahol konkrétan oxálsavat írnak az acetilén vs. permanganát eredményeképp, és ezek szerint itt nem hasad.
Ettől függetlenül persze a megadott képlet - C2H2(OH)2 - se oxálsavra, se hangyasavra nem jön ki.
Viszont:
Az általad idézett Bayer reagenses Wikipédia link reakcióegyenlete nem zárja ki, hogy ecetsav keletkezzen. A slusszpoén az, hogy a C2H2(OH)2, bár nem szokás így felírni (és elég megtévesztő is), de az összegképlet alapján lehet Ecetsav.

Az acetilén valószínűleg a kétoldali csatlakozó láncok hiánya miatt kivétel az alkinok általános viselkedése alól. Az alkinok valószínűleg azért hasadnak ebben a reakcióban, mert az összesen háromszoros oxigénkötés létrejöttéhez valamelyik oldalon hasadnia kell a C-C kötésnek, és az az oldal van jobban célkeresztben, ahol eredetileg a hármas kötés volt. Az acetilénről viszont a hidrogént könnyebb lehet leszedni. Az oxálsavas verzió meg talán azért van, mert bizonyos körülmények közt tovább oxidálódhat.
Ez persze csak feltételezés. Eleve nem értem miért írná valaki úgy le az ecetsavat, hogy két hidroxilcsoportot emel ki. Ez inkább etén-diol lehetne, de annak az esetleges keletkezésére még célzás sincs a forrásokban.
-

becuszabi
aktív tag
válasz
 englandfan
#129
üzenetére
englandfan
#129
üzenetére
A Wikipedia szerint az etin (acetilén) esetén nem ez a vége a reakciónak, mert a szénlánc felhasad és hangyasav, ill. annak kálium-sója keletkezik.
A tartaric acid, magyarul borkősav megint másképpen néz ki. Valami nem kerek abban a feladatban. -

englandfan
csendes tag
Etin kálium-permanganátos vízben való elnyelésekor ezek az anyagok keletkeznek: C2H2(OH)2 + MnO2 + KOH. Az lenne a kérdésem, hogy azt első, szerves anyag az vajon mi lehet? Mert az biztos hogy létezik ilyen, mert a google is ezt adja ki a reakcióegynletre, annyit találtam, hogy tartaric acid... Az biztosan valamilyen sav, ám annak az összegképlete: C4H6O6. És az nem igazán jön ki így...
-

becuszabi
aktív tag
válasz
 Taknyoshal
#127
üzenetére
Taknyoshal
#127
üzenetére
Ha teljesnek tekintjük a Ca-hidroxid disszociációját, akkor 11.
A számítás menetét rád bízom, biztos benne van a könyvben.
...vagy mint mindenben a Google itt is segít
-

Taknyoshal
tag
0.0005 mol/dm3-es koncentrációjú Ca(OH)2 oldatnak mennyi a Ph-ja?

-

Mackósajt
senior tag
válasz
 Taknyoshal
#124
üzenetére
Taknyoshal
#124
üzenetére
Egy reakció során nem feltétlenül bomlik fel minden eredeti kapcsolat a résztvevők közt. Fel lehet ismerni a tipikus csoportokat a sav-bázis reakcióknál.
H2SO4 (kénsav) -> SO4(2-) szulfát
HNO3 (salétromsav) -> NO3(1-) nitrát
stb.Ezeket egyszerűen fel kell ismerni ránézésre, és egyben kezelni.
Annál is inkább fontos, hogy ezeket a molekuláris ionokat felismerd, és egyben kezeld, mert vizes oldatban, ahol a laborban leginkább találkozni lehet ezekkel a reakciókkal, nincs szigorúan vett közvetlen kapcsolat az erős savak anionjai, és a képletben hozzájuk rendelt hidrogénion(ok) között. Az a kötés ilyenkor csak papíron létezik.
-

becuszabi
aktív tag
válasz
 Taknyoshal
#124
üzenetére
Taknyoshal
#124
üzenetére

A reakció eredménye szempontjából a salétromsav oxigénjeinek jelenléte szinte mellékes, mert nem változnak meg a reakció során...mint, ahogy a korábban tárgyalt MgO és H2SO4 reakciójában is a víz képződéséhez a sav adja a protont, az oxid pedig az oxigént (és nem a sav).
...természetesen a salétromsav oxigénjei abból a szempontból már fontos szerepet kapnak, hogy ebben az összetételben egy (nem is akármilyen) erős savval állunk szemben. -

becuszabi
aktív tag
válasz
 Taknyoshal
#122
üzenetére
Taknyoshal
#122
üzenetére
Mert nincs benne oxigén

No, de: bázis és bázis között is van különbség. Több sav-bázis elmélet is létezik. A nitrogén elektronszerkezete nagyon változatos vegyületek képződését teszi lehetővé. Az ammóniában a nitrogénnek történetesen van egy nem kötő elektronpárja, aminek köszönhetően nagyon könnyen elcsíphet egy protont. A salétromsavban ill. a hozzá hasonló klasszikus savakban pedig pont ilyen mozgékony proton van. Ezért reagál savakkal.
-

becuszabi
aktív tag
válasz
 Taknyoshal
#120
üzenetére
Taknyoshal
#120
üzenetére
Ezek ugyanolyanok, mint a ZnO + HCl, sav-bázis reakciók.
Nem történik elektronátmenet, DE tudni kell, hogy mi keletkezik.
Savak és fém-oxidok reakciójában a fémek sója és víz keletkezik.
Az egyenlet rendezéséhez csak annyit kell figyelembe venni, hogy a fém-oxidban a fém milyen oxidációs állapotú, illetve, hogy a sav anionja hány vegyértékű.
Kezdjük ez utóbbival: mivel a savakban a H mindig +1-es ox. állapotú, ezért a sav anionja annyi vegyértékű, amennyi H van benne. Ennek megfelelően a HNO3 anionja -NO3, míg a H2SO4-é pedig =SO4 (a vonalak jelölnék a vegyértéket).
Az ólom és a magnézium egyaránt +2-es oxidációs állapotú (lsd. a korábbi hozzászólásokat az oxigén, oxidokban felvett oxidációs állapotáról).
Az ólom-nitrát képlete így: Pb(NO3)2, a magnézium-szulfáté pedig MgSO4
Az egyenletek:
PbO + 2 HNO3 → Pb(NO3)2 + H2O
MgO + H2SO4 → MgSO4 + H2O -

Taknyoshal
tag
Helló. Bonyolultabb egyenletek esetén továbbra sem értem, pl: pbo+hno3 vagy mgo+ h2so4 köszönöm a türelmet.
-

Mackósajt
senior tag
válasz
 Taknyoshal
#116
üzenetére
Taknyoshal
#116
üzenetére
1. Ez valóban nem mindig egyértelmű, kell hozzá lexikális alap is. Főleg, hogy sokszor nem történik semmi.
2. Tudni lehet, hogy a ZnO-ban a Zn +2, mert ott van mellette az O, ami szinte mindig -2. A Cl pedig szinte mindig -1, az összes többi változata bizonyos ritka vegyületekben fordul elő, amiket fel lehet ismerni.A Cl biztosan nem lehet a "+" pár a Zn mellett, mert sokkal erősebb elektronvonzó (lásd első hozzászólásom). Alapvetően ha két erősen különböző elektronvonzó képességű elem vegyül egy ionos vegyületben (mint amilyen a ZnCl2), akkor az erősebben elektronvonzó elem (Cl) leszakítja a gyengébb elektronvonzó (Zn) külső elektronját/elektronjait, így az erősebb elektronvonzó negatív lesz (Cl(-1)), a gyengébb elektronvonzó pozitív (Zn(+2)). Ha az elektronvonzó képesség közel azonos, akkor osztoznak (kovalens vagy fémes), úgyhogy vissza is jutottunk a hogyan döntjük el milyen kötés kérdéshez.

A Zn, Cl és nagyon sok elem esetén is igaz, hogy elvileg ugyan többféle vegyértékük lehet, de gyakorlatilag ezek közül 1 v. 2 sokkal gyakoribb, mint a többi. Ez különösen igaz a periódusos táblázat két szélén lévő elemekre, a középen lévők lelkivilága sajnos bonyolultabb, mert az elektronszerkezetük külső része elég trükkös. Innentől mint mondtam játszik a lexikális tudás. Sok mindent ki lehet logikázni, de nem mindent.
Azt kell megérteni, hogy az elemek a vegyületek létrehozásakor arra "törekednek" (elhatárolom magam a saját durva antropomorfizmusomtól
 , hogy lezárják az elektronszerkezetüket, a nemesgázokéhoz hasonló zárt szerkezetet hozzanak létre. Amelyik elem ezt úgy éri el könnyeben, hogy az utolsó zárt héj fölötti elektronokat leszórja (a periódusos rendszer bal oldala) az ezt fogja "tenni", amelyik úgy éri el könnyebben, hogy befog még pár elektront, és lezárja az utolsó réteget (a jobb szél) az ezt fogja tenni. A periódusos rendszerben benne van az elektronszerkezet is, tessék tanulmányozni. Kiderül belőle mennyi elektronnak kell mozognia egy adott helyzetben.
, hogy lezárják az elektronszerkezetüket, a nemesgázokéhoz hasonló zárt szerkezetet hozzanak létre. Amelyik elem ezt úgy éri el könnyeben, hogy az utolsó zárt héj fölötti elektronokat leszórja (a periódusos rendszer bal oldala) az ezt fogja "tenni", amelyik úgy éri el könnyebben, hogy befog még pár elektront, és lezárja az utolsó réteget (a jobb szél) az ezt fogja tenni. A periódusos rendszerben benne van az elektronszerkezet is, tessék tanulmányozni. Kiderül belőle mennyi elektronnak kell mozognia egy adott helyzetben.Vagy olvasgatni: [link] Én ezt a könyvet annyira nem szeretem, de el tudom képzeli, hogy másnak hasznos lehet.
Kezdek kicsit zavaros lenni talán. Ma korán megyek aludni.

Honnan tudom? Hát ahhoz jól hangzó "master of chemistry"-hez vezetett egy kis út.
 Más kérdés, hogy az utolsó 8 évben csak felejtettem, de mindent még nem sikerült.
Más kérdés, hogy az utolsó 8 évben csak felejtettem, de mindent még nem sikerült.2 másodperc...
-

becuszabi
aktív tag
válasz
 Taknyoshal
#116
üzenetére
Taknyoshal
#116
üzenetére
1. Ehhez kell megtanulni és megérteni a kémiát. Felismerni, hogy az adott reakció milyen jellegű.
A korábbi FeO+ Al példában például redukciós-oxidációs (vagy röviden redox) folyamatok zajlottak le.
A ZnO + HCl esetén ilyen nem történik, tehát minden marad az eredeti oxidációs állapotában.
ZnO + 2 HCl → ZnCl2 + H2O, ez egy úgynevezett sav-bázis reakció.
2. Az, hogy két olyan elemből, aminek több oxidációs állapota is lehet, a végén milyen vegyület jön létre az sok mindentől függ. Mint sok más esetben itt is elő lehet szedni az elemek elektronegativitás értékeit. Ha a lehetséges vegyület alkotói között nagy a különbség, akkor szinte biztos, hogy a nekik megfelelő szélsőséges értéket fogják felvenni. Például a fémek, amelyek elég könnyen megszabadulnak az elektronjaiktól egy halogénnel nagy valószínűséggel olyan vegyületet alkotnak, amelyben a lehető legmagasabb oxidációs állapotban vannak jelen. Sokszor persze a körülményektől is függnek, hogy milyen vegyület jön létre ... pl, az átmeneti fémek között több variáció is lehet egy vegyület összetételére (lsd. a vas-oxid is egy ilyen)....és, hogy honnan? Kb. 15 évig ezt tanultam, vegyész vagyok...és gyanítom, hogy Mackósajt személyében is egy kollégát köszönthetek

-

Taknyoshal
tag
válasz
 Taknyoshal
#116
üzenetére
Taknyoshal
#116
üzenetére
2. kérdést talán értem. Nem azért, mert az oxigén miatt a cinknek 2-es oxidációs számmal kell szerepelnie?
Különben Ti honnan értitek ezt ennyire?

-

Taknyoshal
tag
-

Mackósajt
senior tag
válasz
 Taknyoshal
#113
üzenetére
Taknyoshal
#113
üzenetére
Az előttem szóló részletes magyarázatához csak annyit fűznék hozzá, hogy imádtam a laborban az aluminotermikus reakciót, szép vulkánt lehetett vele csinálni.
 Persze a kohászatban nem vas-oxiddal csinálják, mert a drágább alumíniumot áldozod be az olcsóbb vas kinyerésére. Króm előállítására viszont jó, és asszem a vasútnál használják sínforrasztásra a vasoxidos változatot is.
Persze a kohászatban nem vas-oxiddal csinálják, mert a drágább alumíniumot áldozod be az olcsóbb vas kinyerésére. Króm előállítására viszont jó, és asszem a vasútnál használják sínforrasztásra a vasoxidos változatot is.Egy általános tanács: ha komolyan meg akarod érteni a miérteket a kémiai kötésekben és a reakcióegyenletek rendezésében, akkor periódusos rendszer a legjobb barátod. Először azt értsd meg, hogy miért úgy vannak elrendezve abban a táblázatban az elemek, ahogy. Ha ez megvan, akkor a szervetlen kémia egy csomó kérdése (köztük az általad feltett kettő) sokkal egyszerűbben megérthetővé válik. Egy nyomtatott periódusos rendszer szintén nagy segítség, pl. a vegyértékszámok kinézhetőek belőle az egyenletrendezéshez.
Vannak elemek, amelyeknek többféle vegyértéke is lehet. Ilyen a példaegyenletben szereplő vas is, amely lehet +3 vagy +2. Mint az becuszabi hozzászólásából is kiderül, onnan lehet tudni, hogy egy vegyületben mennyi a vegyértéke, hogy mi van mellette. Az oxigén mindig -2 (na jó, szinte mindig
 , így az FeO-ban a vasnak +2-nek kell lennie, máskülönben nem lenne semleges. Lehetne Fe2O3 is, abban +3 a vas. A reakció remekül megy vele, tipikusan ezzel csinálják a termitet. Ebben az esetben.
, így az FeO-ban a vasnak +2-nek kell lennie, máskülönben nem lenne semleges. Lehetne Fe2O3 is, abban +3 a vas. A reakció remekül megy vele, tipikusan ezzel csinálják a termitet. Ebben az esetben.Fe2O3 + 2 Al = Al2O3 + 2 Fe
-

becuszabi
aktív tag
válasz
 Taknyoshal
#113
üzenetére
Taknyoshal
#113
üzenetére
Talán Mackósajt nem haragszik meg.
Szóval:
az egyenlet rendezése nem ördöngősség, mert csak a négy alapműveletet kell használni
DE azért persze tudni kell hozzá a kémiát is, hiszen a példa egyenletet fel lehetne írni úgy is, hogy: FeO + Al → Fe + AlO, ami persze nem jó, mert olyan vegyület, hogy AlO nem létezik.
Tudni kell, hogy milyen reakcióról van szó és milyen anyagok keletkezhetnek.
A mi esetünkben a vas-oxid alumíniummal történő redukciójáról van szó, aminek az eredménye elemi vas és alumínium-oxid.
Az elemi vas 'képletével' nincs gond, az ugye Fe. Az alumínium-oxid képletéhez (ha nem tudjuk fejből) elő kell szedni pl. egy periódusos táblát, amin feltüntetik az elemek lehetséges oxidációs állapotait. Alumíniumnál ez +3. Az oxidokban az oxigén oxidációs állapota -2 (persze mint mindenhol van egy két kivétel, de azokat most hagyjuk). Ahhoz, hogy az alumíniumból és az oxigénből létrejövő anyag 'semleges' legyen a +3-as oxidációs állapotú Al-ból kell 2, a -2-es ox. állapotú O-ből pedig kell 3, így az alumínium-oxid képlete Al2O3.
Most, hogy már megvan a képletünk, csak osztani, szorozni kell.
A FeO + Al → Fe + Al2O3 egyenlet rendezéséhez az oxidációs állapotok változásait kell figyelembe venni. A 'semleges' Fe-oxidban ha az oxigén oxidációs állapota -2 (lsd. fentebb), akkor a vasé +2. Az elemi vasban az oxidációs állapot ugyebár nulla, tehát a reakció során a vas felvesz 2 elektront. Az Al ugyanekkor a nulla oxidációs állapotból úgy jut el a +3-asba, hogy lead 3-at.
Az egyenlet rendezéséhez a leadott és felvett elektronok számát egyenlővé kell tenni. Mi az az egész szám, ami 2-vel és 3-mal egyaránt osztható? A 6, tehát úgy kell rendezni az egyenletet, hogy 6 elektron átmenete történjen meg. 1 Fe(+2) felvesz 2-őt, ahhoz, hogy 6 elektron felvétele legyen, kell 3 Fe(+2), azaz 3 FeO. Az Al(0) → Al(+3) állapotváltozás 3 elektront jelent, a 6-hoz kell két Al.
Nézzük meg az egyenletünket:
3 FeO + 2Al → 3 Fe + Al2O3
A biztonság kedvéért persze a végén számoljuk meg, hogy az egyes elemek száma megegyezik-e a két oldalon. -

Mackósajt
senior tag
válasz
 Taknyoshal
#111
üzenetére
Taknyoshal
#111
üzenetére
Úgy érted ott van előtted egy ismeretlen anyag, és arról megmondani vagy ott van előtted egy képlet, és arról megmondani? Az utóbbi eset az egyszerűbb, a periódusos rendszerek (és a Wikipédia) tartalmazzák az elemek elektronegativitását. Ha az összetevők elektronegativitása közti különbség nagy (pl. NaCl), akkor ionos, ha a különbség kicsi, de maguk az elektronegativitások nagyok (pl. NO vagy O2), akkor kovalens, ha a különbség kicsi, és az elektronegativitások is kicsik (pl. Fe magában), akkor fémes. Ha nem szimplán elemekből tevődik össze, hanem egyik vagy másik ion maga is molekula (pl. NaHCO3) akkor bonyolultabb az ügy, fel kell ismerned a tipikus molekuláris ionokat lexikális ismeret alapján, mondjuk itt is alkalmazható az az ökölszabály, hogy erős elektronvonzó képességű elemek (C, O, -> CO3), gyenge elektronvonzó képességű elemek (Na) mellet ionos kötést sugallnak akkor is, ha valamelyik ion belül kovalens.
Ehhez nem kell ismerni a pontos számokat, az elektronegativitás a periódusos rendszer jobb felső sarkában a legnagyobb (nemesgázok nem számítanak!), és a bal alsóban a legkisebb, a középső tartományokban pedig alig van különbség a szomszédok között.
Hogy miért van így, az túlmutat egy ilyen hozzászóláson, az atomok elektronszerkezetét (energiaszintek, árnyékolás) kell hozzá megérteni.
Ha egy ismeretlen anyag van előtted, és arról kell megmondanod ionos vagy fémes, arra nincs univerzális módszer az összetétel ismerete nélkül. Mondhatnám, hogy az ionosak jobban hajlamosak vízben oldódni érthető módon, de vannak olyan ionos vegyületek, amelyek csak azért se.
-

Taknyoshal
tag
Hogyan tudom megállapítani valamiről, hogy milyen kötése van? (ionos vagy kovalens)
Help. -

becuszabi
aktív tag
Nem, olyan magas koncentrációról nincs szó, mint pl. a szódavíznél...szóval nem pezseg

Néhányszor 10 mg/l-es értékről van szó. Ennyit fel tud oldani a víz. Természetesen ha nyitva hagyod a palackot, akkor idővel csökken a mennyisége.A neten böngészve, sokan sok mindent állítanak a hatásosságáról.
-

becuszabi
aktív tag
Egyszerűen oxigént buborékoltatnak át rajta. Ha szükséges, akkor mindezt meg lehet tenni nyomás alatt, esetleg a víz hűtése közben, mivel mindkét körülmény javítja az oldhatóságot.
Hétköznapi példa: szódavíz (csak ott szén-dioxid van a vízben).Amúgy nem nagyon látom értelmét a dolognak. Nem tudom, hogy jelent-e bármilyen előnyt a gyomorba bevitt oxigén (fizikailag van a vízben, felszívódás közben nem jut tovább), de ha igen, akkor is az egészet agyoncsapják a mesterséges íz- és színezőanyagokkal. Nekem parasztvakításnak tűnik.
-

brownus
veterán
üdv,
adva van a víz, ami h2o, ezt, hogy lehet oxigénnel dúsítani? mert most mutatott egy kolléga egy palack o-val dúsított vizet... a tecsóban árulják.... finom alma és kiwi ízesítésű cucc
-

becuszabi
aktív tag
Ne aggódj, jobban belemélyedve a dolgokba több ellentmondásra is lelhetsz

Itt például a héjakon található elektronok száma másképpen van megadva. Ez egyébként is egy elmélet, így vannak körülötte bizonytalanságok.
(...az f-mező elemei amúgy is elég "különc" társaságot alkotnak) -

ngabor2
nagyúr
a 4-5-6. héjon levő alhéjak energiái igen közel vannak egymáshoz, mint látható, a 6s energiája alacsonyabb, mint az 5d, vagy a 4f pályáé. nem nagyok a különbségek, igen könnyen gerjesztődnek egyikről a másikra. valamikor régen tudtam a sort, hogy hogyan következnek egymás után, a 4. héjtól igen nagy kavarok voltak.
-

jasszer
őstag
Sziasztok,
Kémiából kaptam egy egyszerű feladatot, a cérium elektronszerkezetét kell meghatározni, a vegyértékhéj megjelölésével. Elkezdtem töltögetni a héjakat, úgy éreztem hogy minden f*sza, aztán ránéztem a periódusos rendszerre, ahol [Xe]4f2 6s2-nek jelölik. Mit rontottam el?

A szaggatott vonal feletti terület lenne a vegyértékhéj...
Új hozzászólás Aktív témák
- Hobby elektronika
- Napelem
- Milyen alaplapot vegyek?
- Mibe tegyem a megtakarításaimat?
- Itt a Galaxy S26 széria: az Ultra fejlődött, a másik kettő alig
- Kerékpárosok, bringások ide!
- Xiaomi 15 - kicsi telefon nagy energiával
- Motoros topic
- AliExpress tapasztalatok
- Windows 11: miért nem vált mindenki?
- További aktív témák...
- AKCIÓ ÚJ Bontatlan Macbook Pro 16 M4 MAX 14 32GPU 36GB 1TB Magyar billentyűzet Azonnal átvehető Deák
- AKCIÓS ! MacBook Pro 16" M1 Pro 16GB RAM 512GB SSD! 1 év garancia!
- EVGA RTX 3080 10GB GDDR6X FTW3 ULTRTA GAMING Eladó!
- Dell Latitude 5490 14",FHD,i5-8350U,8GB,256GB SSD,WIN11
- Synology Plus 16TB - HAT3310-16T - Új - Eladó!
- AKCIÓ! Asrock B450M R5 5500 8GB DDR4 256GB SSD GTX 1050 Ti 4GB Zalman T3 Plus DeepCool 400W
- GYÖNYÖRŰ iPhone 14 Pro Max 256GB Deep Purple-1 ÉV GARANCIA - Kártyafüggetlen, MS4398, 100% Akksi
- HIBÁTLAN iPhone SE 2020 64GB White -1 ÉV GARANCIA - Kártyafüggetlen, MS4307, 100% Akksi
- Laptop felvásárlás , egy darab, több darab, új , használt ! Korrekt áron !
- Samsung Galaxy Watch 4 LTE 6 hónap Garancia Beszámítás Házhozszállítás
Állásajánlatok
Cég: Laptopműhely Bt.
Város: Budapest


 Belelógattam a cérnát a túltelített oldatba, aztán vártam a csodát (hogy gyönyörű kristályok legyenek rajta), végül megfeledkeztem róla (több hét) és a só kimászott
Belelógattam a cérnát a túltelített oldatba, aztán vártam a csodát (hogy gyönyörű kristályok legyenek rajta), végül megfeledkeztem róla (több hét) és a só kimászott 




























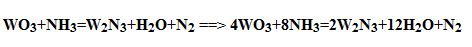






 arikázd be a nem létezőket!
arikázd be a nem létezőket!